

科研动态

前列腺素是生物体内一系列具有独特生物活性的小分子化合物,其通常来自于生物体内环加氧酶等对花生四烯酸的氧化代谢。该类分子结构上,一般具有高度取代的五元环核心、连续稠密的手性中心以及复杂多变的氧化态;而功能上,其对血压、凝血、生长、生殖等生理活动具有重要的调节功能,与疼痛、炎症、发热等病理过程也密切相关。到目前为止,已有超过20个前列腺素类药物被批准用于各类疾病的治疗,全球年销售额达数十亿美元,市场巨大、需求广泛。因此,发展简洁高效的路线来合成前列腺素类分子,对满足市场需求、降低用药成本、助力新药研发或具有重要意义。
近期,上海交通大学变革性分子前沿科学中心长聘教轨副教授、张江高等研究院入驻科学家李健团队报道了一条基于化学酶法高效合成前列腺素类分子的新路线,实现了几种具代表性前列腺素类分子的高效合成;其中对于天然前列腺素PGF2α,该路线实现了5步10克规模的合成,这成为该分子距今报道过的最短合成路线之一(图1)。不同于传统的Corey lactone 合成方案,该团队基于化学酶法和自由基切断策略,设计了Corey lactone自由基等价物8共同中间体,以生物酶催化精准构建了分子的手性中心,通过廉价金属Ni催化高效偶联了分子侧链。相关研究以“A concise and scalable chemoenzymatic synthesis of prostaglandins“为题发表于Nature Communications,2022级博士生殷允鹏和访问学者王金鑫为论文共同第一作者,李健副教授为论文通讯作者,上海交通大学变革性分子前沿科学中心为论文第一通讯单位。
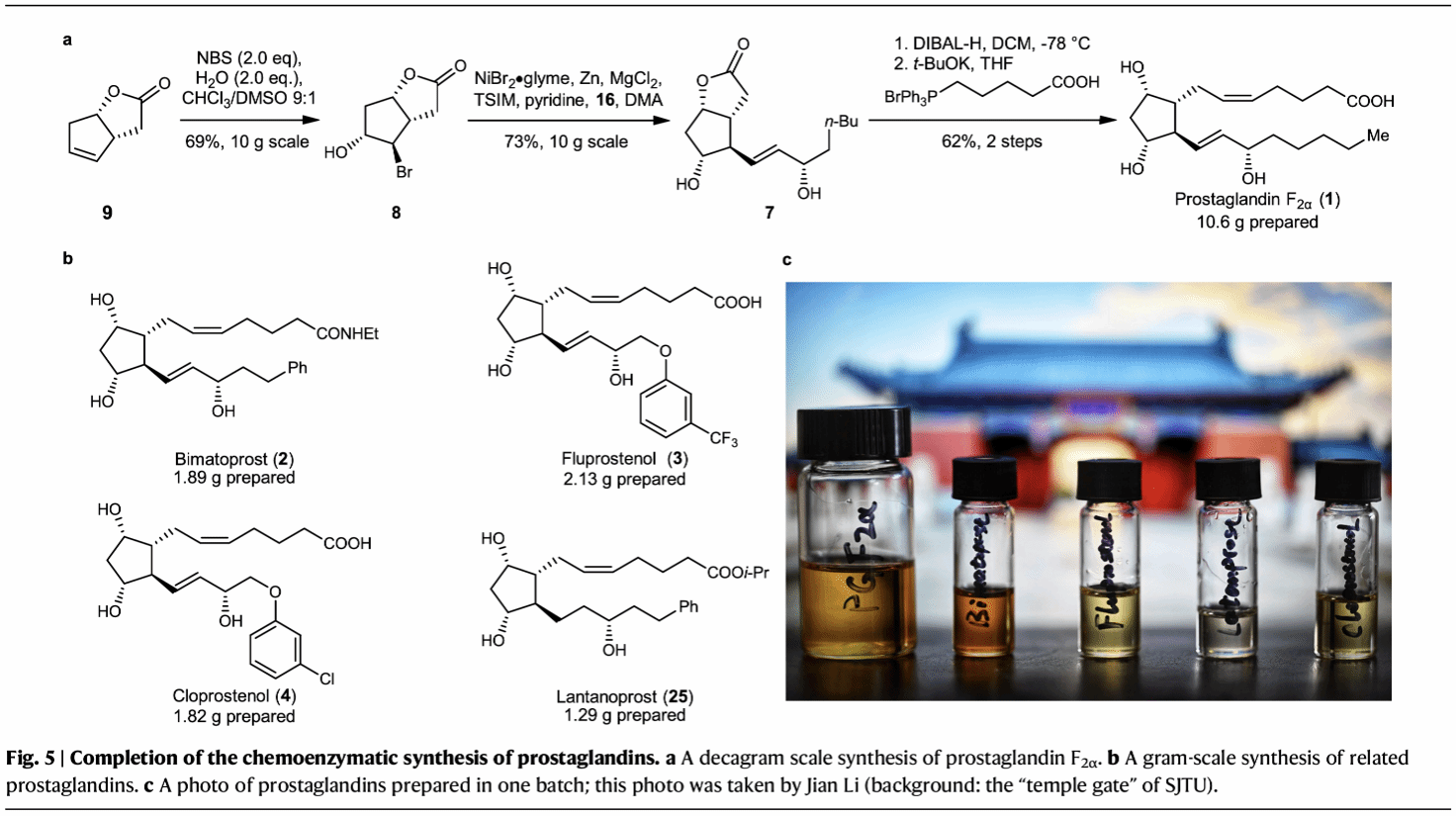
图1 前列腺素类分子的合成路线
基于化学酶法和自由基切断策略,作者对该类前列腺素分子进行了如下的逆合成分析(图2),其中PGF2α (1) 的a侧链可由Wittig反应快速组装;w侧链可由廉价金属Ni催化的还原偶联反应直接对接(自由基切断);Corey lactone自由基等价物8则是对化合物9的双键直接羟溴化获得;而对于化合物9,可分别通过BV酶的不对称拆分(体内酶催化)和脂肪酶去对称化(体外酶催化)产品11进行Johson-Claisen重排获得。
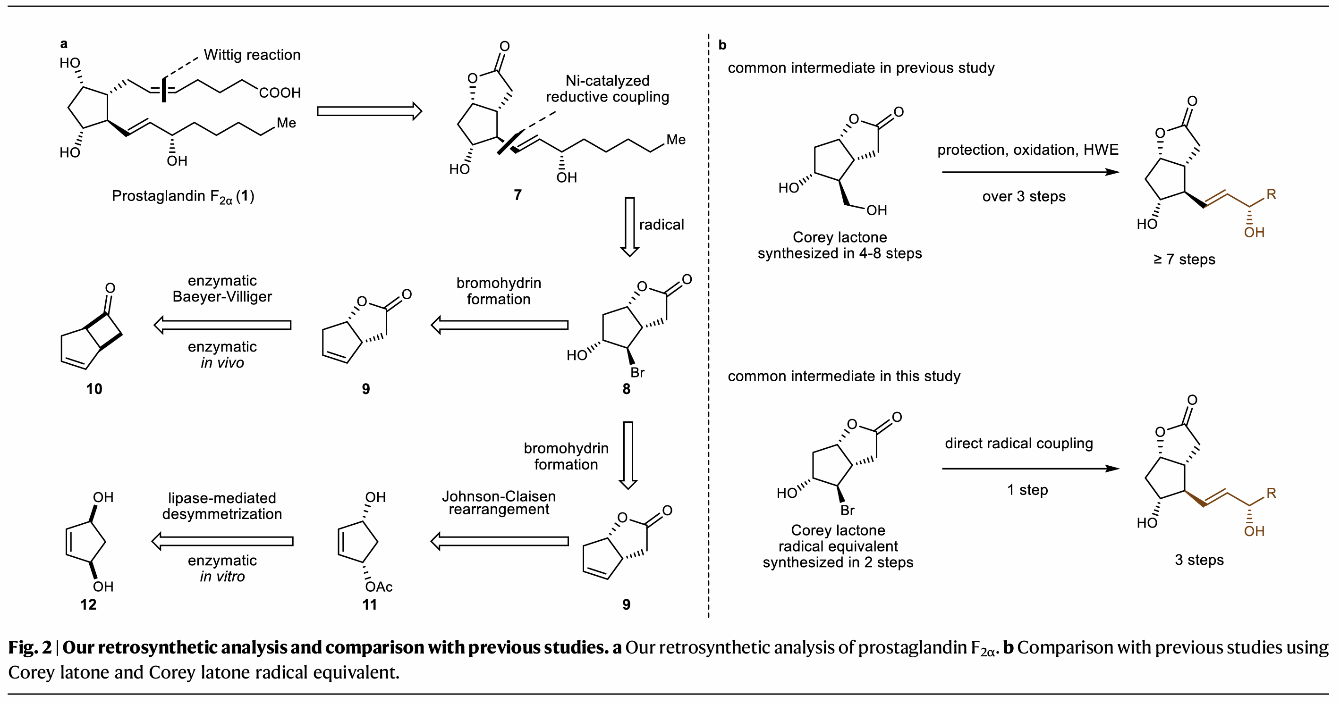
图2 前列腺素类分子的逆合成分析
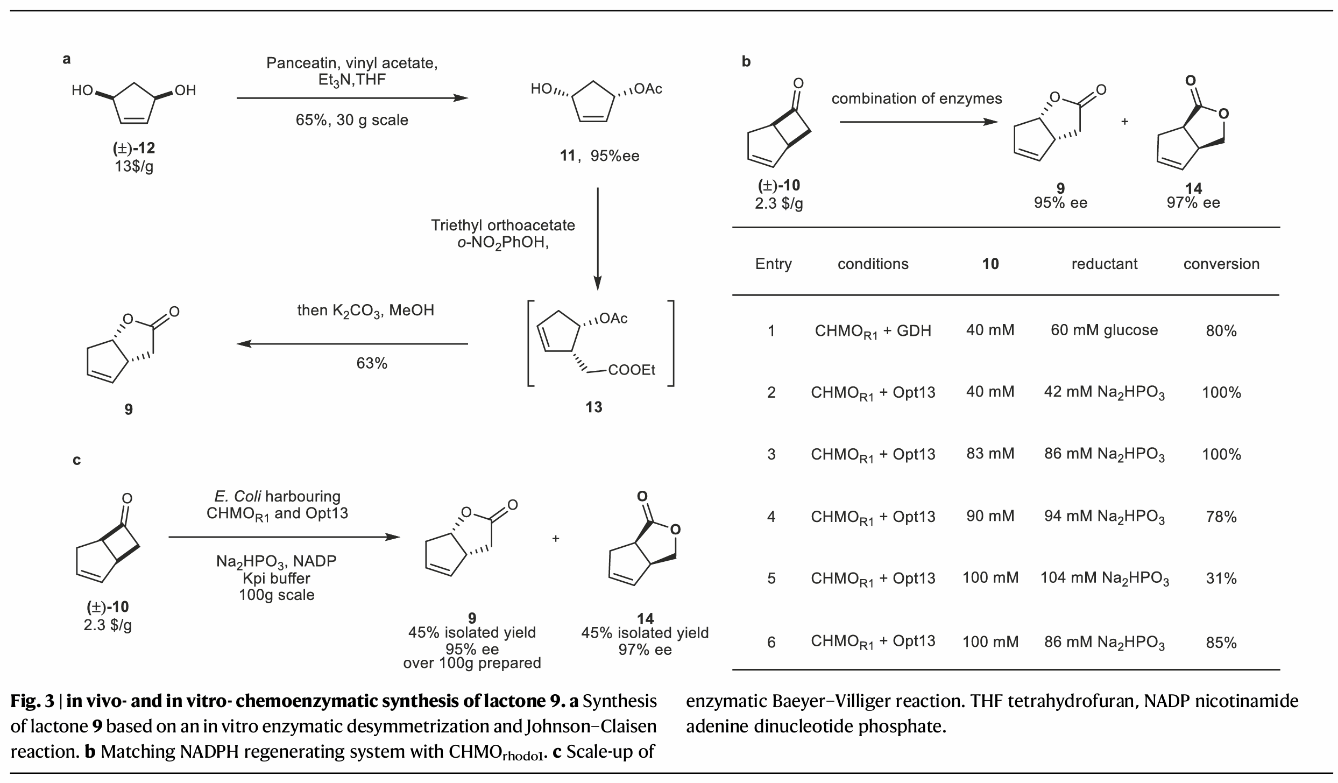
图3 BV酶催化的不对称拆分
该工作中,作者通过构建Opt-13 NADPH再生系统替代GDH NADPH再生系统,使得体系浓度达到9.3 g/L,并在实验室条件下实现化合物9的100克规模制备(图3);利用混合溶剂体系下DMSO作Lewis碱催化的羟溴化实现了对Corey lactone自由基等价物8的更高选择性的制备(图4);通过对Weix与龚和贵团队发展的Ni催化还原偶联反应体系的具体优化,实现了10克规模下对邻羟基烷基溴化物与烯基溴化物的高效偶联(图4)。
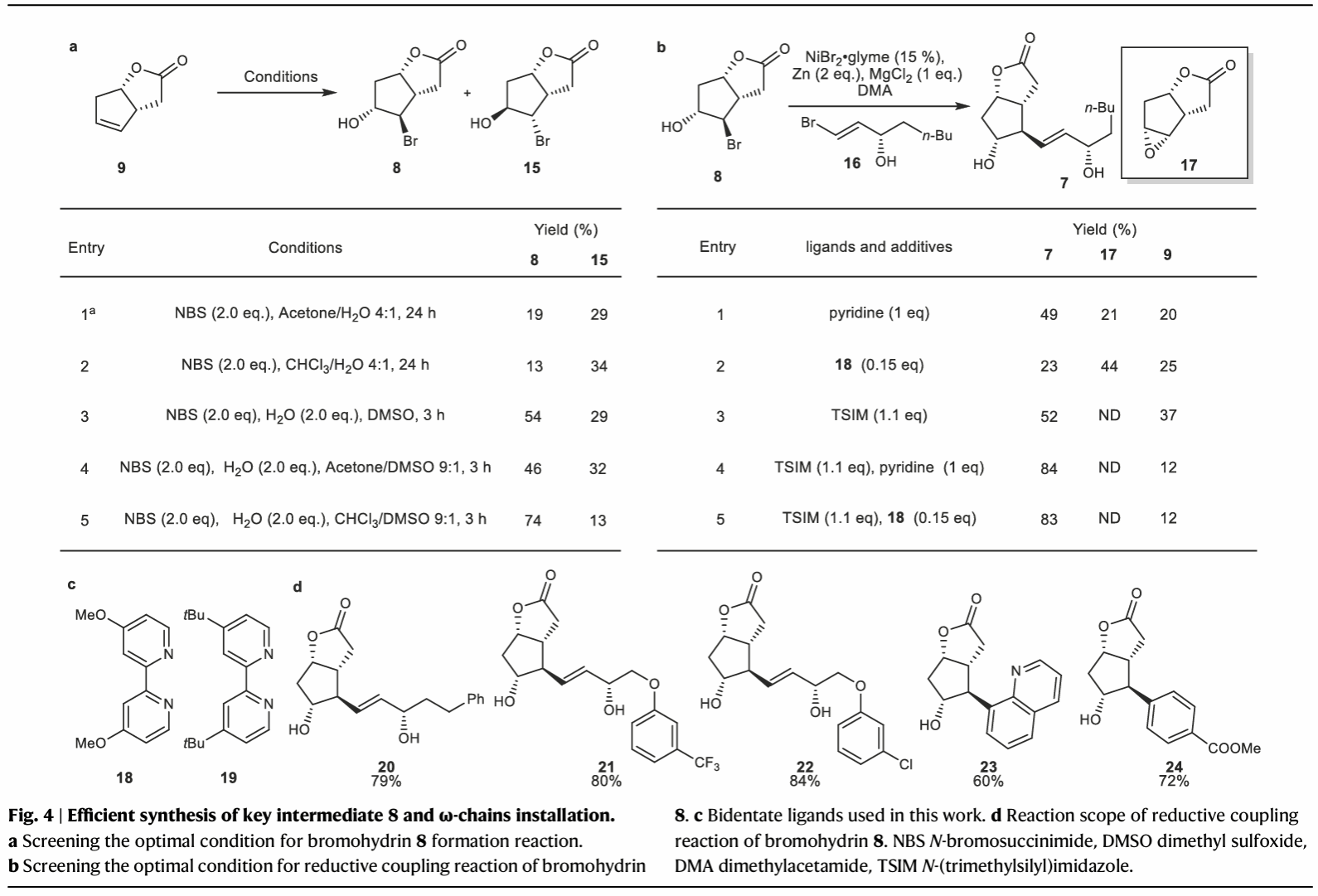
图4 羟溴化和Ni催化的还原偶联反应
综上所述,李健团队基于化学酶法和自由基切断策略,以Corey lactone自由基等价物8为共同中间体,实现了5-7步对几种具代表性前列腺素类分子的高效合成,其中5步实现对天然前列腺素PGF2α 的10克规模的合成,是该分子距今报道过的最短合成路线之一;此外,基于该合成策略,也可以实现对其他一些新型前列腺素类似物的快速合成。该研究或能够为满足当下前列腺素类分子药物的市场需求、降低用药成本、助力新药研发提供具有潜力的新方案。
该工作得到了国家重点研发计划、上海市青年科技启明星计划、中央高校基本科研经费的资助;李昂和Hans Renata教授为该工作提供了宝贵的建议,林双君教授为该工作无私的提供了实验室和设备支持。
【原文链接】https://doi.org/10.1038/s41467-024-46960-y





 交大主页
交大主页